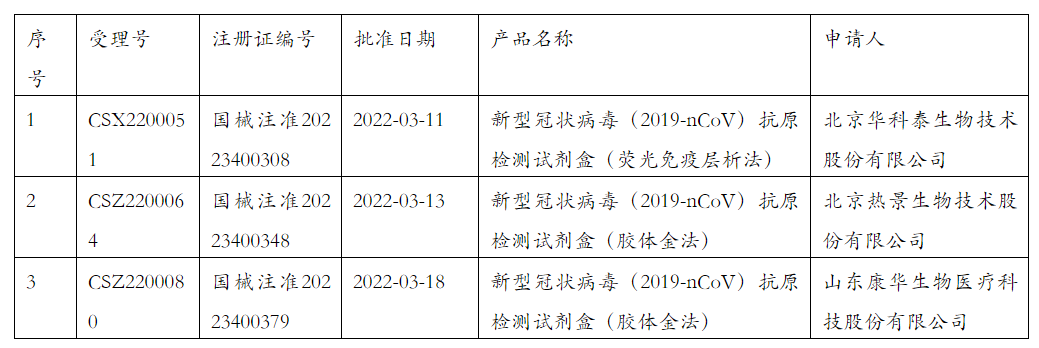
伴随着新冠自测政策的出台,中央应对新型冠状病毒感染肺炎疫情工作领导小组日前决定在核酸检测的基础上,增加抗原检测作为补充,并组织制定了《新冠病毒抗原检测应用方案(试行)》。截止3月18日,累计有17家企业申报的新型冠状病毒(2019-nCoV)抗原检测试剂盒被国家药品监督管理局审批通过,3家海达投资企业北京华科泰生物、北京热景生物、山东康华生物申报产品获批。
北京华科泰生物作为首批获批的“新型冠状病毒(2019-nCoV)抗原检测试剂盒(荧光免疫层析法)”,采用创新的干式荧光微球标记技术及创新的信号采集处理技术,使抗原检测的灵敏度和特异性大大提升。按照中国国家药监局的三类医疗器械审批标准,在国内3家临床机构完成临床试验,入组病例共计510 例,产品与新冠核酸检测结果的总符合率达89.80%(95%CI:86.87%,92.14%),临床性能表现优异。
被股民称为科创板年度“预增王”的北京热景生物于第二批获批“新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)”。热景生物是一家专注于体外诊断行业、致力于发展新型体外诊断技术与创新产品、推动医学检验与POCT产业融合发展的国家级生物技术高新企业,同时也是一家致力于癌症早筛的医疗服务企业。2021年3月2日,热景生物新冠抗原自我检测试剂获德国药监局批准上市,成为国际第一批新冠自我检测产品批准上市的企业,而后又先后获得CE和多个国家批准,在德国、法国、意大利、英国、奥地利、比利时、荷兰、越南、泰国、文莱等30多个国家上市,已成为欧洲家庭自我检测市场主流产品,受到广泛认可。近日,热景生物新冠抗原自测试剂在新加坡获批上市。
此次山东康华生物获批的新型冠状病毒抗原检测试剂盒通过检测从受检者采集的口咽、鼻咽拭子或鼻拭子以确定受检者是否存在新型冠状病毒感染。无论是从操作的简便性和结果的准确性上,都更加满足当前新冠病毒检测需求。在全球疫情防控中,康华&汉唐新型冠状病毒抗原快速检测试剂成为强有力的检测工具,相继获得德国保罗埃利希研究所(PEI)性能验证、德国联邦药品和医疗器械机构(Bfarm)注册证、欧盟自测CE证书、澳大利亚TGA认证等多国权威认证,出口70多个国家和地区。相信在当前国内疫情形势依然十分严峻的情况下,康华生物将继续发挥作用,为疫情防控贡献力量!